近日,我所生物技术研究部高分辨分离分析及代谢组学研究组(1808组)许国旺研究员等,与大连医科大学附属第一医院乐卫东教授、邵亚平教授及广州医科大学附属脑科医院王静教授等合作,通过整合代谢组学、蛋白质组学与宏基因组学,系统绘制了伴快速眼动睡眠行为障碍的帕金森病(RBD-PD)这一临床侵袭性亚型的独特分子图谱,揭示了RBD-PD患者血液中的显著富集是源自肠道菌群的毒性芳香族氨基酸分解代谢产物,并构建了一个包含9种代谢物的诊断模型,区分帕金森病亚型,为理解疾病异质性、早期预警及精准干预提供了新视角。
PD是一种起病隐匿、病因复杂的神经退行性疾病,现有诊断主要依赖运动症状的出现,但此时患者脑内已发生不可逆的病理损伤。PD的早期诊断及精准干预是当前临床的难题。RBD作为PD最特异的前驱症状之一,与PD的核心病理标志α-突触核蛋白的异常聚集密切相关,且合并RBD的PD患者往往表现出更严重的自主神经功能障碍、更快速的运动功能恶化及更早发的认知减退,被视为一种进展迅速的PD恶性亚型。因此,RBD为认识和干预PD早期神经退行性病变提供了重要窗口。
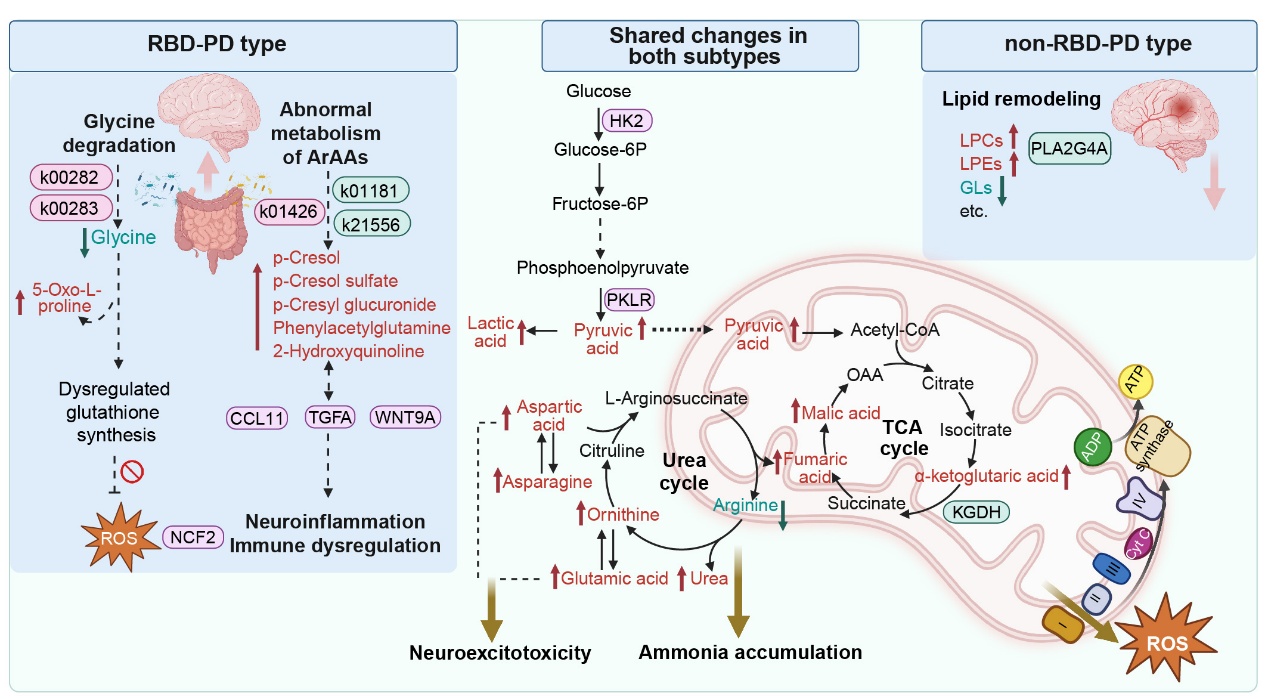
在本工作中,科研人员利用两个独立的临床研究队列,通过多平台代谢组学发现,RBD-PD亚型肠道微生物群衍生的毒性蛋白质降解产物(例如对甲酚及其衍生物、苯乙酰谷氨酰胺和5-氧代-L-脯氨酸等)会出现显著累积的现象,且在PD前驱期(RBD阶段)即已出现。科研人员通过联合靶向蛋白质组学进一步发现,这些代谢变化与加剧的氧化应激和神经炎症关联。此外,科研人员通过整合宏基因组分析揭示,上述代谢异常是与肠道菌群功能从“膳食纤维发酵”向“芳香族氨基酸、甘氨酸和肠道黏液层降解”转变密切相关。这些发现证明了菌群失调驱动的代谢重编程不仅是RBD时期的关键分子事件,更可能是驱动其向PD演进的核心病理机制。
基于上述发现,科研人员构建了一个包含对甲酚硫酸盐、甘氨酸、5-氨基戊酸等9种代谢物的诊断模型。该模型在区分RBD-PD与非RBD-PD患者时,在发现和验证队列中分别表现出0.826和0.967的曲线下面积,有望为实现PD的精准分型提供有力工具。
我所1808组与大连医科大学附属第一医院乐卫东团队长期致力于基于代谢组学的神经退行性疾病生物标志物发现、致病机制解析和创新治疗方法研究,先后构建了辅助阿尔茨海默症(AgingDis.,2020)和帕金森病(Mol Neurodegener.,2021)诊断,以及早期风险预测的生物标志物模型。基于SOD1G93A转基因动物,合作团队揭示了嘌呤代谢异常在肌萎缩侧索硬化症疾病演化中的关键作用(Neurobiol Dis.,2023),并结合国内多中心临床队列发现次黄嘌呤和肌苷在肌萎缩侧索硬化症识别中的临床转化价值(Chin Med J (Engl).,2026);系统绘制了能量限制条件下多脑区的动态代谢谱(Signal Transduct Target Ther.,2023)等,为能量限制改善神经退行性疾病的分子机制提供了数据支撑。
上述研究以“Distinct metabolomic and proteomic signatures in Parkinson’s disease patients with REM sleep behavior disorder”为题,发表在《信号转导与靶向治疗》(Signal Transduct Target Ther.)上。该工作的共同第一作者为我所已毕业博士邵亚平、广州医科大学附属脑科医院王静。该工作得到国家自然科学基金、上海市中央引导地方科技发展资金、大连市科技创新人才等项目的资助。(文/图 邵亚平)






