近日,我所生物技术研究部生物分子高分辨分离分析及代谢组学研究组(1808组)许国旺研究员、胡春秀副研究员等,与大连医科大学附属第二医院王琪教授、北京大学王玮教授等合作,利用自主研发的高效循环肿瘤细胞(CTC)捕获平台结合单细胞代谢组学技术,基于CTC代谢特征,对肺癌转移的潜在风险进行推测,有望为肺癌转移早期预警和个体化治疗提供新工具。
肺癌的高死亡率主要归因于肿瘤的转移倾向,而现有影像学和组织病理学诊断方法难以在临床症状出现前预测转移,亟需非侵入性生物标志物来识别高风险患者,并指导个性化治疗。CTC是原发性肿瘤脱落后进入血液循环的转移“种子”,也是液体活检的关键靶标。传统CTC检测技术存在诸多局限,且操作过程会破坏细胞活性,导致后续功能与分子分析难以实现。
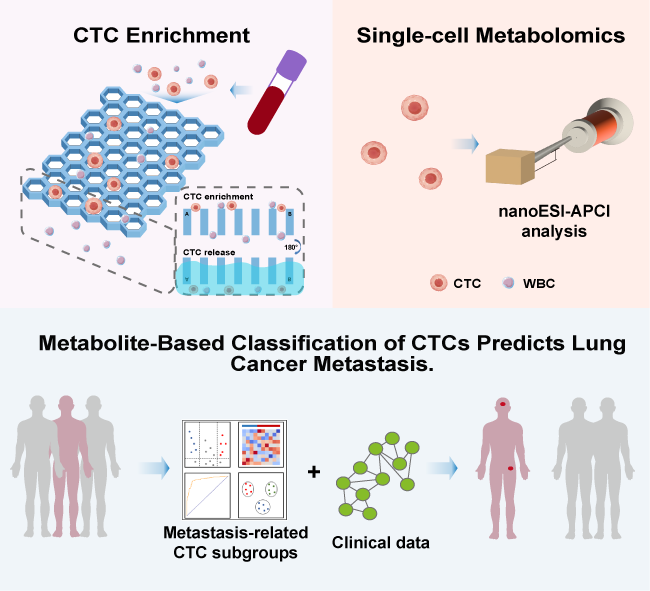
本研究针对CTC检测的技术瓶颈,开发出基于负向富集与聚对二甲苯C(Parylene C)微孔阵列膜的CTC分选捕获平台,同时实现了高捕获效率(大于 89%)与细胞高活性保持率(大于 87%)。科研人员利用同轴纳升电喷雾电离-大气压化学电离质谱(nanoESI-APCI MS)技术,对来自临床患者和动物模型的301个CTCs进行了单细胞代谢组学分析,鉴定出390种代谢物,发现脑转移倾向CTC中苯丙氨酸代谢异常升高、骨转移倾向CTC中精氨酸生物合成通路激活的特征性“代谢指纹”。
基于上述发现,科研人员构建的CTC代谢分型模型,将CTC划分为不同转移风险亚组,其预测性能优于传统临床指标和CTC计数,对脑转移和骨转移的预测准确率(AUC)分别达0.74和0.92。前瞻性临床验证证实,该模型可提前6至11个月预警转移事件。该成果为肺癌转移风险预测提供了新方法。
相关研究以“Prediction of Lung Cancer Metastasis Risk Based on Single-Cell Metabolic Profiling of Circulating Tumor Cells”为题,发表在《先进科学》(Advanced Science)上。该工作共同第一作者为大连医科大学博士研究生徐阳、袁媛和我所1808组博士研究生胡学森。该工作得到国家重点研发计划、国家自然科学基金、大连医科大学附属第二医院-中国科学院大连化学物理研究所医工联合基金、我所创新基金等项目的资助。(文/图 胡春秀、徐阳)
文章链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202508878






