近日,我所生物技术研究部生物分子结构表征新方法研究组(1822组)王方军研究员团队利用自主搭建的极紫外激光解离质谱仪器系统,探究了酰基载体蛋白(ACP)在活化过程中,以及其与C4至C18不同链长脂肪酰基相互作用的分子机制,揭示了酰基链长依赖的ACP构象动力学机制,为ACP结构理性进化和脂肪酸生物合成链长调控提供了理论指导。
ACP在脂肪酸生物合成中起着核心作用,负责携带、保护并转运不断延长的脂肪酰基链。解析ACP适配和稳定不同链长酰基底物的构象动力学过程对于阐明脂肪酸链的稳定、延伸及释放分子机制至关重要。然而,ACP及其酰基化中间体具有高度的结构动态性和化学不稳定性(尤其是硫酯键易水解),现有实验表征技术难以对其进行高选择性、高灵敏度表征。
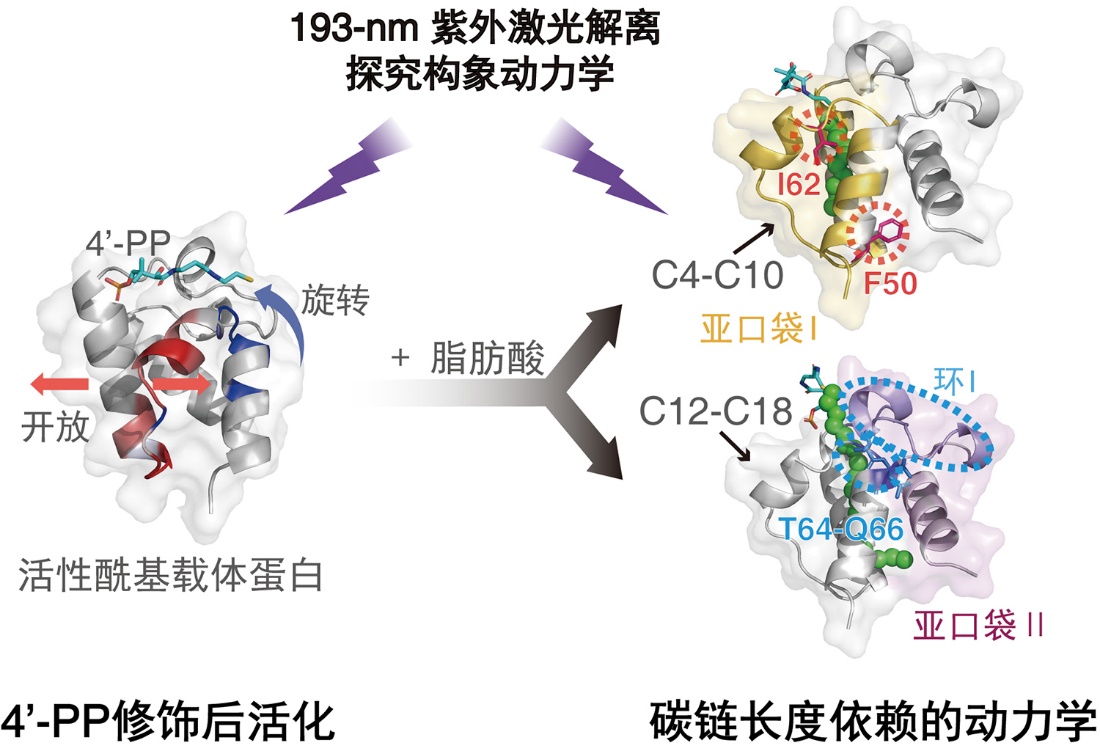
本工作中,研究团队采用非变性质谱(nMS)实现对不稳定酰基化ACP中间体在离子阱中的高选择性富集,并进一步采用193-nm极紫外光解离(UVPD)技术,实现对其构象动力学特征的高灵敏度表征。研究发现,酰基链首先插入ACP的疏水性亚口袋I中,直到链长超过10个碳原子(大于C10)后,过长的疏水碳链会发生弯曲并进入亚口袋II。结构分析发现,Phe50和Ile62两个关键氨基酸位点在调节ACP疏水口袋尺寸方面起着关键性作用,而Loop I及Thr64-Gln66区域对于稳定长酰基链(C12-C18)至关重要。该工作不仅为理解ACP对酰基链长度的调控机制提供了分子层面的新见解,也为通过理性设计改造ACP结构以提高目标脂肪酸如中链脂肪酸(C8-C12)的生物合成效率提供了理论指导。
近年来,王方军团队致力于极紫外激光解离质谱新仪器、新方法的自主研发及其在生物大分子结构功能研究中的前沿应用,尤其在蛋白质结构动力学、蛋白质相互作用、药物作用机制、蛋白质-纳米材料界面表征等领域取得了系列进展(J. Am. Chem. Soc.,2025;J. Am. Chem. Soc.,2024;Chem. Sci.,2024;Nat Protoc.,2023;J. Am. Chem. Soc.,2023;J. Am. Chem. Soc.,2023)。
相关研究成果以“Ultraviolet Photodissociation Mass Spectrometry Captures the Acyl Chain Length-Dependent Conformation Dynamics of Acyl Carrier Protein”为题,于近日发表在《美国化学会志》(Journal of the American Chemical Society)上。该工作的共同第一作者是我所联合培养硕士研究生谢沅芝和刘哲益副研究员。该工作得到了国家重点研发计划、国家自然科学基金、我所创新基金等项目的资助。 (文/图 谢沅芝)






