近日,我所本草物质科学研究室(二十八室)卿光焱研究员、梁鑫淼研究员团队在糖链纳米孔单分子分析方面取得新进展。团队提出并验证了一种“单特征”纳米孔识别策略:通过在蛋白纳米孔内构建协同识别微区,实现了对α2–8糖苷键的位点特异性识别。进一步结合纳米孔兼容的前处理方法与机器学习,该团队在血清基质中实现了对α2–8糖链的识别与定量,展示了糖苷键导向的纳米孔糖链分析方法的应用潜力。
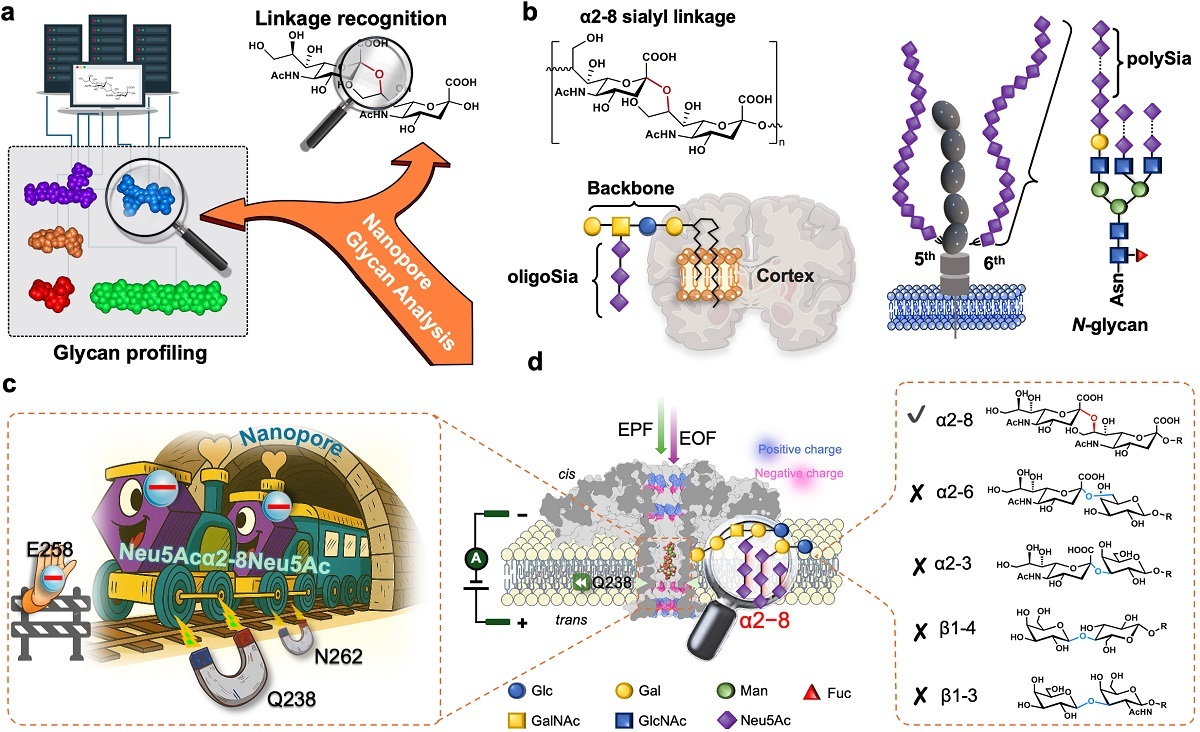
细胞表面糖缀合物在诸多生理与病理过程中发挥重要作用,但其结构表征长期受制于糖链的组合复杂性。单糖种类、连接位点(1–2、1–3、1–4、1–6)、α/β构型及分支等因素导致结构空间呈指数级增长,超出了传统参考谱库与“指纹式”分析的能力。纳米孔单分子传感技术为糖链分析提供了新的可能,但当前的纳米孔糖组学多以“指纹式”分析为主,依赖糖链转运过程中的电流阻塞图谱来推断其组成与连接方式。然而,糖链的高维复杂性使得这一策略面临天然局限:不同结构产生的电学信号高度相似,甚至单个羟基方向的微小差异都可能导致特征重叠。当样本复杂度增加时,传统的匹配识别方法迅速失效。因此,为实现从轮廓分析向序列级糖组学的转变,亟需新的理论框架与技术方案。
卿光焱等长期致力于推动纳米孔单分子传感技术在复杂糖链分析中的应用(Chem. Sci., 2020; Nat. Commun., 2023;ACS Nano, 2024; ACS Nano, 2024;Nano Lett., 2025;Angew. Chem., 2025),在此基础上,本工作中团队提出针对某一亚类糖链的“单特征”识别方法,选择α2–8唾液酸链作为靶标,该糖链在神经发育、膜微区、肿瘤与衰老等过程中具有明确的生物学意义,同时,其结构相似性高,对纳米孔检测平台的分辨能力提出了较高要求,为评估高分辨率测试平台的性能提供了合适的研究对象。
团队通过在蛋白纳米孔内工程化非共价互作位点,实现对糖苷键的位点选择性识别。以工程化aerolysin K238Q为例,其在孔内N262–Q238–E258协同识别微区可特异“读取”α2–8糖苷键:Gln238与Asn262提供多点氢键/接触,而暴露的Glu258构成静电屏障,共同延长糖链的易位时间,从而在单事件尺度上区分二、三、四α2–8寡唾液酸及其主链变体,并排除α2–3/α2–6与中性糖链。同时,K238N变体对更长链或高度分支的寡糖链表现互补响应,并可与K238Q构成双孔逻辑门测定体系,用于快速提取未知糖链的关键结构信息。结合水相兼容的血清预处理与基于卷积神经网络的智能纳米孔数据分析模型,本体系在复杂基质中实现了a2-8糖链的单事件级识别与半定量分析。该工作为纳米孔技术从“指纹式”识别向“位点感知”和“序列化”糖组学的发展提供了新思路,有望为纳米孔在生物与临床糖链分析中的应用奠定概念基础。
相关研究成果以“Single-Feature Identification of α2–8 Linked Sialoglycans Using Engineered Aerolysin Nanopores: A Paradigm for Glycan Linkage Analysis”为题,于近日发表在《美国化学会志》(Journal of the American Chemical Society)上。该工作的第一作者是二十八室博士后李佳齐。上述工作得到了国家自然科学基金、国家重点研发计划、我所创新基金等项目的资助。(文/图 李佳齐)






